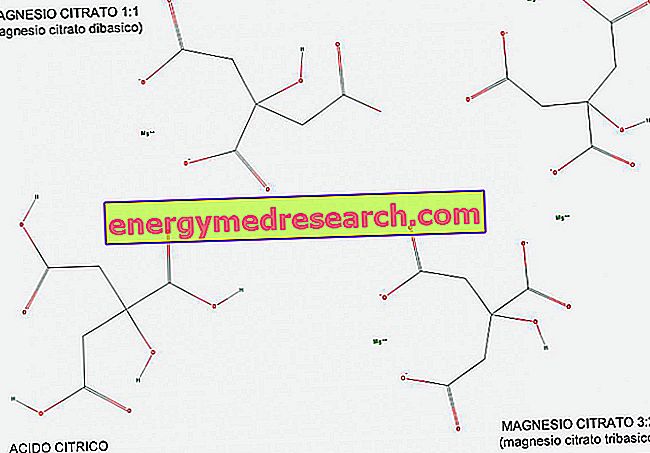
एक ट्राइबैसिक (या ट्राइप्रोटिक) एसिड एक एसिड होता है जो एसिड-बेस प्रतिक्रिया में तीन हाइड्रोजन आयनों को दान करने के लिए होता है। आकृति की मदद से हम देख सकते हैं कि साइट्रिक एसिड, ट्रिबैसिक एसिड का एक उदाहरण है, क्योंकि इसमें तीन COOH कार्बोक्जिलिक समूह हैं जो आसानी से एच हाइड्रोजन प्राप्त कर सकते हैं।
मैग्नीशियम साइट्रेट दोनों 1: 1 अनुपात (1 मैग्नीशियम अणु प्रति साइट्रेट अणु) में मौजूद है, और 3: 2 अनुपात में (3 मैग्नीशियम अणु प्रति 2 साइट्रेट अणु)।
मैग्नीशियम साइट्रेट 1: 1 को डिबेसिक कहा जाता है क्योंकि यह साइट्रिक एसिड का डिबासिक नमक है; वास्तव में, इसके 2 अणु मूल समूह (COO-) प्रति अणु हैं, जो 2 कार्बोक्जिलिक समूहों से प्राप्त होते हैं जिन्होंने प्रतिक्रिया के दौरान अपने हाइड्रोजन को छोड़ दिया।
दूसरी ओर, मैग्नीशियम 3: 2 को ट्राइबेसिक कहा जाता है क्योंकि इसमें 3 अकार्बनिक मूल समूह (COO-) प्रति अणु होते हैं, जो 3 कार्बोक्जिलिक समूहों से प्राप्त होते हैं जिन्होंने प्रतिक्रिया के दौरान अपने हाइड्रोजन को छोड़ दिया।
ट्राइबेसिक मैग्नीशियम साइट्रेट स्पष्ट रूप से मैग्नीशियम (वजन से 42.6%) अधिक समृद्ध है, डायबासिक मैग्नीशियम साइट्रेट की तुलना में; इसके अलावा, यह अधिक क्षारीय है, क्योंकि यह तीन हाइड्रोजन आयनों एच + को दो के खिलाफ स्वीकार कर सकता है। हालांकि यह पानी में कम घुलनशील है।



